科学探索|西湖大学蔡尚团队首次证实细菌是乳腺癌转移的重要帮凶( 二 )
结果显示,清除肿瘤菌群之后,肿瘤重量并没有受到影响,但肺转移显著下降 。这表明,肿瘤菌群很可能影响的不是肿瘤的生长,而是转移过程 。
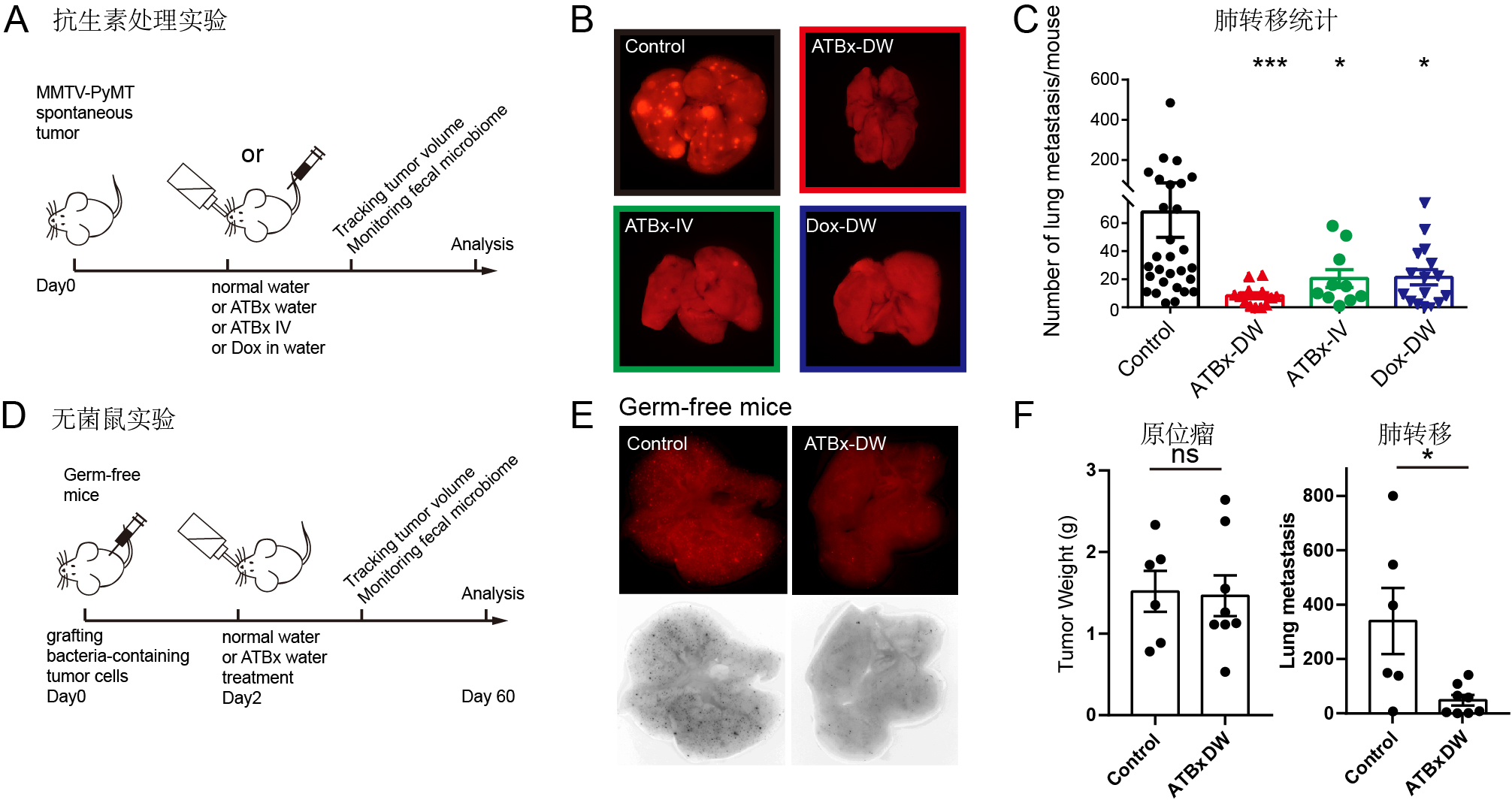
文章图片
抗生素清除实验证明肿瘤菌群对于肿瘤转移非常重要
基于此发现,研究团队提出假设:肿瘤组织中的胞内菌会和肿瘤细胞一起迁移到达远端器官并影响转移 。也就是说,肿瘤里的细菌会跟着肿瘤细胞一起跑到身体的其他部分 。
为了验证这个假设,他们对原位肿瘤、肉眼可见的肺转移灶、含有微小转移灶的肺组织、以及正常的肺和乳腺组织进行细菌16S测序 。分析结果显示,早期肺转移的细菌可能仍带有原位肿瘤的菌群特征,而随着肿瘤的生长、扩散,渐渐开始受肺部微环境的影响 。
再通过分离并染色循环肿瘤细胞,研究团队看到循环肿瘤细胞能够带着胞内菌“跑到”远端器官;而回输这些胞内菌到肿瘤细胞内,可以看到肿瘤细胞在人体内“跑动过程中的生存能力更强”,甚至那些不容易转移的乳腺癌,在输入胞内菌以后,也开始转移 。
这就有力地证明了胞内菌可以促进肿瘤细胞的转移 。
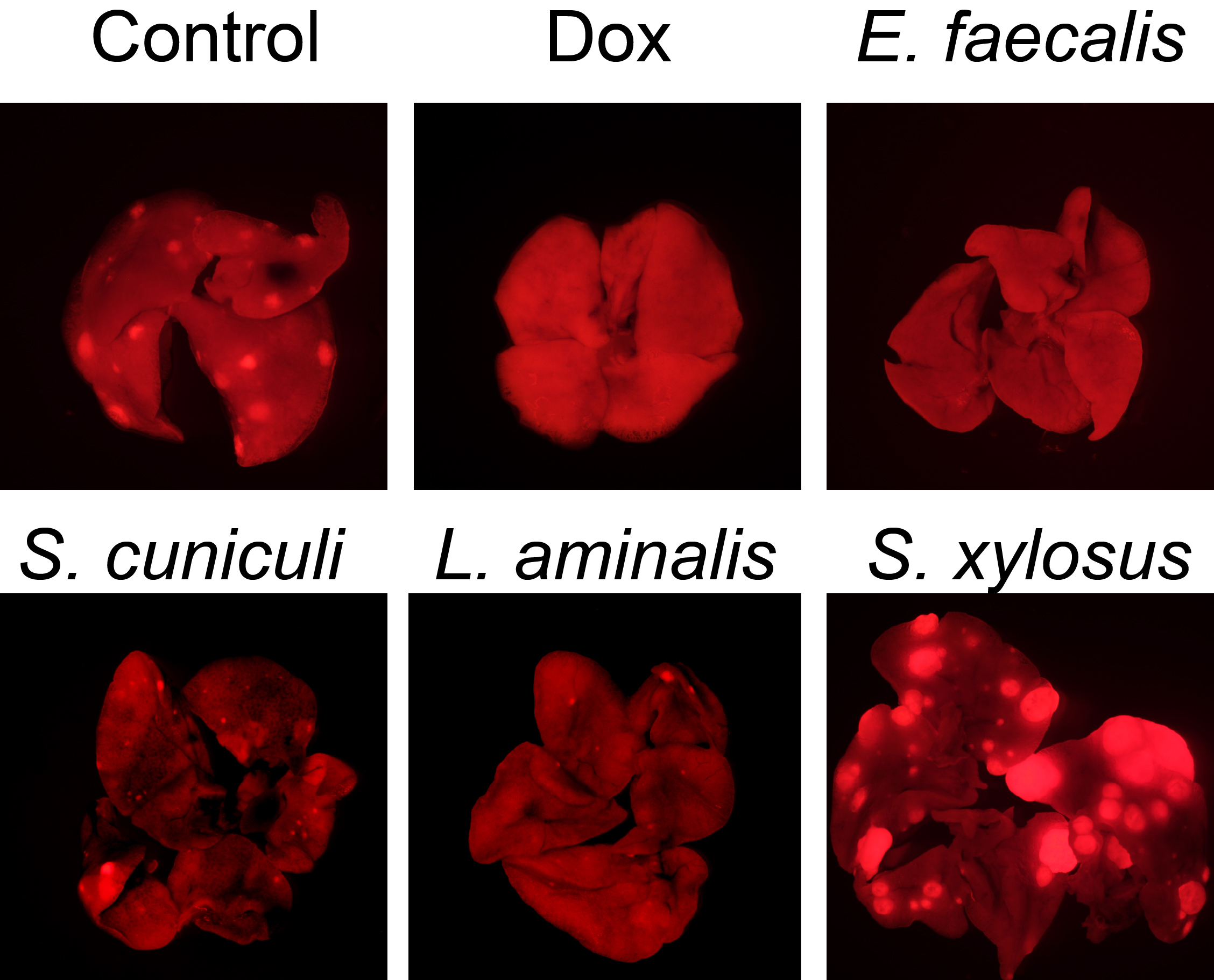
文章图片
细菌回输促进乳腺癌转移
知其然,知其所以然 。为什么胞内菌可以促进肿瘤细胞转移?
蔡尚解释说,事实上,在转移过程中,癌症细胞没有我们想象中那么“威力无边”,血管里的血压(液流压力)会对它造成损伤 。但他们发现,胞内菌入侵肿瘤细胞后,会通过特定的信号通路(RhoA-ROCK)来重塑细胞骨架,帮助肿瘤细胞抵抗血管里的压力,避免转移过程中受到损伤 。
这就完美解释了为什么拥有胞内菌的肿瘤细胞拥有更强的能力跑到远端器官 。
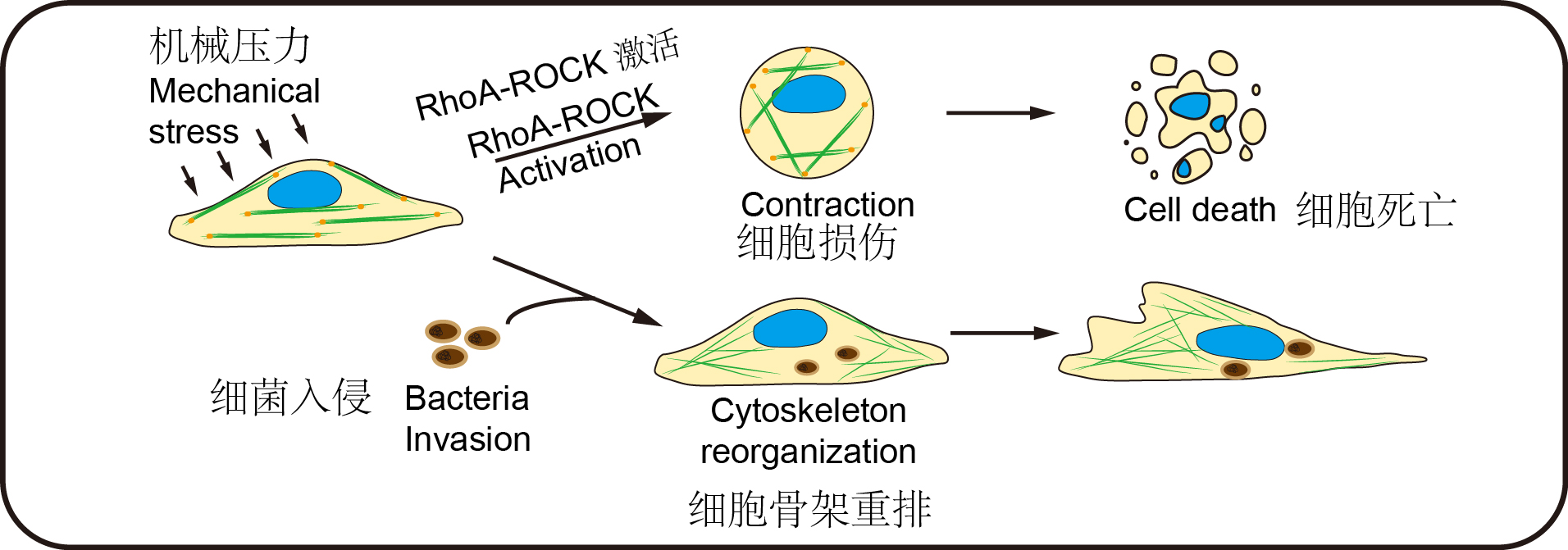
文章图片
胞内菌的入侵重塑了肿瘤细胞的细胞骨架,以此来抵抗液流压力的模式图 。
最后,研究团队从小鼠回归到人体,收集了配对的乳腺癌病人的肿瘤组织、癌旁组织和淋巴结组织,用qPCR结合16S测序定量和定性地分析各自菌群的组成 。结果显示,小鼠乳腺癌组织和人乳腺癌组织具有相同的微生物谱和动态变化,这表明,人乳腺癌菌群可能在人癌症发生和进展中起着相似的作用 。
历时近5年,从猜想、假设到一步步证实,蔡尚团队的研究鉴定了肿瘤微环境中长期被忽视的新成分,揭示了影响肿瘤转移的新因素,开拓了肿瘤研究的新方向,为临床控制肿瘤转移提供了全新的视角 。
西湖大学生命科学学院蔡尚研究员为论文的通讯作者;西湖大学生命科学学院博士后付爱坤,西湖大学博士生尧冰清和董婷婷为本文的共同第一作者 。此外,西湖大学高性能计算中心李南老师、黎航老师对本课题做出了重要贡献 。本课题受到国家自然科学基金委的资助;课题实施过程中得到了西湖实验室、西湖大学实验动物中心、生物医学实验技术中心、高性能计算中心的大力支持 。
一场历时5年的探险
看到研究结果的那一刻,蔡尚很兴奋 。
“这个课题风险很大,充满未知,当我决定启动研究的时候,连肿瘤菌群是否真的存在都极具争议 。”蔡尚说 。
最初的idea来自蔡尚在斯坦福做博士后时的一次探讨:什么基因在影响乳腺癌肿瘤的发展 。“构建诱导敲除基因的小鼠模型时,我意外地发现不需要敲除这个基因,只需要加入诱导剂(一种抗生素),肿瘤的转移就会受到影响 。我觉得很不可理解 。”
- 科学探索|科学家研发毫米级机器人 可实现人体内靶向给药
- 科学探索|野生蝙蝠被发现可在4年后识别跟食物奖励相关的铃声
- 科学探索|盘点大自然6种能使身体部位再生的动物
- 科学探索|中国空间站的光学舱:巡天空间望远镜预计2024年投入科学运行
- 科学探索|科学家发现了本质上不会衰老的物种
- 科学探索|问天实验舱器箭组合体今天进行垂直转运
- 科学探索|新研究揭示了大象是如何避免癌症的
- 科学探索|一种新开发的抗生素被发现可以杀死耐药性细菌
- 科学探索|增材纺织法造出人工心室模型
- 科学探索|MIT团队找到改善工业沸水工艺的方法
